Points Reco – Fibrillation atriale ESC 2020
Définitions de la FA
o FA = Tachycardie supra ventriculaire avec activité atriale non efficace (électrique et mécanique)
⇒ Sur ECG : Intervalles RR irréguliers ou Absence d’ondes P et activation atriales irrégulières
o FA clinique = Présence continue sur > 30 sec des signes ECG de FA (sur 1 dérivation) ou un ECG 12 dérivations compatible
o FA subclinique/AHRE = Cas où signes de FA/flutter atrial/Tachycardie atriale détectés par un pacemaker/holter ECG ou par une montre connectée dont le tracé fourni est vérifié
(mais ne suffisant pas pour le diagnostic de FA clinique)
– R1 : Le diagnostic d’une FA est fait sur un ECG 12 dérivations qui montre des signes de FA sur > 30 sec
o Pas d’ondes P
o Intervalles RR irréguliers– R1.b : La détection d’un évènement type FA doit faire vérifier le tracé fourni par le pacemaker/holter/montre connectée.
Epidémiologie de la FA
– 1ère cause d’arythmie cardiaque
o En augmentation dans le monde
o Prédomine dans les pays occidentaux (Amérique / Europe)
– Pas de score prédictif de FA chez les sains
Présentation clinique et conséquences
- – 50-87% sont asymptomatiques initialemento Possible plus mauvais pronostic dans ce cas
- – Concernant les AVC liés à une FA
o Souvent plus sévères, avec décès/incapacité
o Souvent à répétition
o Possibles emboles systémiques
- – Concernant la défaillance VG
o Risque d’insuffisance cardiaque ↗
o Mêmes facteurs de risques entre la FA et l’insuffisance cardiaque
o Présence des 2 augmente fortement la mortalité cardio vasculaire
- – Concernant les hospitalisations
o 30% des patients avec FA en auront une
o Causes d’hospitalisation des patients FA
▪ 1er : Troubles cardiovasculaires ▪ 2ème : Tb non cardiaques
▪ 3ème : Saignements
- – Concernant les décès chez patients FA :
o 1ère cause = Insuffisance cardiaque aigue
o 2ème et 3ème cause : Cancer/Sepsis
o 4ème cause : AVC
Types de FA, évolution
Types de FA
Evaluation globale d’un patient FA
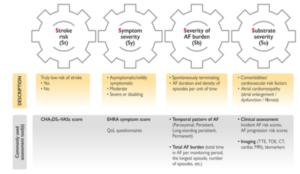
– R2. : Evaluation structurée d’un patient en FA est recommandée en 4 parties (cf. schéma suivant)
– « AF Burden » = Durée d’arythmie par unité de temps sur une FA paroxystique
o Augmentation durée/fréquence des épisodes de FA semble associés à augmentation des évenements thrombo emboliques
o Cependant, pas de lien évident
⇒ Ne doit pas guider le traitement.
Evolution de la FA
- – Passage à une FA persistante est lié à remodelage/ Aggravation de la cardiopathie rythmique
- – Facteurs de risque de passage à une FA persistante o Age élevé
o Insuffisance cardiaque
o HTAo Insuffisance rénale chronique o BPCO
o Diabète
o ATCD d’AVCo Taille de l’oreillette gauche - – Passage en FA permanente est associée à augmentation des complications / décès
Dépistage de la FA
- – FA asymptomatique est associée à augmentation risque d’AVC et de mortalité
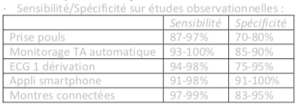
– Outils disponibles :
R3 : Recommandations de dépistages de la FA
– R3.a = Dépistage chez âge > 65 ans
▪ Par la prise de pouls ou un « ECG rythm strip »
▪ Si positif, confirmer par ECG 12 dérivation
– R3.b = Dépistage par ECG 12 dérivations d’emblée si :
▪ Age > 75 ans
▪ Risque élevé d’AVC
Bilan initial d’un patient diagnostiqué avec FA
Figure : Mécanismes de la FA étudiés selon la modalité d’imagerie utilisée. TEE/TOE = ETT/ETO. EP mapping = Etude électrophysiologique.
– Score EHRA = Score d’intensité des sympto
1 = Aucun sympto de la FA
2a = Sympto ne gênant pas les AVQ
2b = Sympto ne gênant pas les AVQ, mais patient gêné par les sympto
3 = Sympto gêne les AVQ
4 = Arrêt total des AVQ
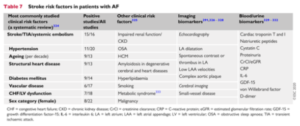
– Facteurs en imagerie prédictifs d’un AVC
o Contraste spontané dans l’OG
o Diminution de la charge de l’OG
o Faible vitesse sanguine dans l’auriculede l’OG
o Configuration non en « aile de poulet » de l’auricule de l’OG
Prise en charge thérapeutique d’une FA
– Prise en charge en 3 parties : ABC
o A : Anticoagulation
o B : Better symptom management
o C : Cardiovasculair/Comorbitities optimization
Anticoagulation (sur FA sans pathologies valvulaires)
Mesure du risque d’AVC sur FA
- Calcul du CHA2DS2-VASc (…/9) ++++o Sexe féminin : Risque similaire aux hommes si score = 1 (équivalent au score = 0 chez un homme)MAIS la présence d’un autre facteur non lié au sexe augmente plus le risque d’AVC chez une femme (score ≥ 2 chez ♀) que chez un homme (score ≥ 1 chez ♂)

– Autres scores / marqueurs biologiques en cours d’études
(⇒ Potentiel pour distinguer ceux à faible risque sur le CHA2DS2-VASc)– Présence d’autres facteurs prédictifs d’AVC mais sont soit
o Inclus indirectement dans le CHA2DS2-VASc
o Dont le lien avec les AVC n’est pas clair
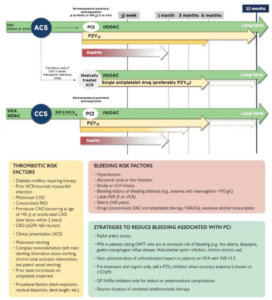
Mesure du risque d’hémorragie
- – Mesuré par le score HAS-BLED
o Meilleur score comparé aux scores biologiques ou autres
⚠ Un score HAS-BLED élevé ne doit pas contre indiquer systématiquement les anticoagulants (mais modifier la PEC par ↘ facteurs modifiables ou ↗ suivi des patients …)
– Bien réévaluer le risque hémorragique pendant le suivi du patient (↗ risque hémorragique lors de la modification des facteurs de risque hémorragique du patient)
Traitements anticoagulants disponibles
Anticoagulants oraux
– Anti vitamine K
o Nécessité d’un bon contrôle INR (>70% du temps dans la cible INR) pour être aussi efficace/sécuritaire que les AOD
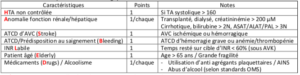
o Score prédictif d’une difficulté à contrôler l’INR = SAMe-TT2R2
▪ (Sexe feminin | Age < 60 ans | ≥ 2/9 ATCD parmi HTA, Diabète, Coronaropathie, AOMI, Insuff cardiaque, AVC, insuffisance pulmonaire, insuffisance rénale, insuffisance hépatique | Traitement | Tabac [2 pts] | Race (non caucasien) [2 pts]
▪ Score ≥ 3 = Risque de mauvais contrôle INR : Soit :
-
- Contrôles plus rapprochés de l’INR
- Utilisation d’un AOD
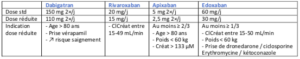
– Anticoagulants Oraux Directs
o A préférer en cas de facteur de risque de mauvais contrôle INR (AOD supérieurs aux AVK dans ce contexte là)
o AOD ont un meilleur profil de tolérance dans
▪ Personnes âgées ▪ Insuff rénale
▪ AVC précédent
⇒ Mais adapter doses d’AOD selon les cas précis
– Autres antithrombotiques
o Double anti-agrégant plaquettaire (AAP) ⇒ Moins efficace que AVL/AOD, mais risque hémorragique équivalent. → Mais utile chez patients avec CI aux anticoagulants (avec double AAP)
o ⚠ Aspirine seule inutile ++
– Combinaison AAP + Anticoagulants ⇒ Ne diminue pas le risque embolique, mais augmente le risque hémorragique
Fermeture de l’auricule
– Par voie percutanée =
o Efficacité non inférieure comparée aux AVK (dont diminution risque hémorragique)
o Utile si contre-indications aux anticoagulants
o Pas d’études d’anticoagulation post geste, mais semble nécessaire
 ⚠ Si contre-indication aux AAP ⇒ Fermeture auricule par voie chirurgicale (ou cathéter épicardique Lariat®)
⚠ Si contre-indication aux AAP ⇒ Fermeture auricule par voie chirurgicale (ou cathéter épicardique Lariat®)
– Par voie chirurgicale ⇒ Réalisé souvent lors des chirurgies à cœur ouvert o Peu de RCT sur cette technique, dont un en cours.o Pas de comparaison entre fermeture auricule et AVK/AOD
Stratégies d’anticoagulation
Stratégie thérapeutique selon l’évolution de la FA
– FA non paroxystique est plus à risque embolique. (tout comme les FA sub cliniques sont moins à risques)
⇒ Mais type de FA ne doit pas affecter la stratégie d’anticoagulation.
Contrôle du risque hémorragique
Diminution du risque hémorragique
– AVK : Contrôle INR en restant > 70% dans index thérapeutique
– AOD : Adéquation posologique
– Eviter prise d’AINS ou d’AAP si possible
– Augmenter fréquence de suivi chez les patients à haut risque hémorragiquePopulations à risque élevé de complications de FA
= Age élevé / Démence / Saignement récent / Insuffisance rénale terminale / Insuffisance hépatique / Cancer…
Populations à risque élevé de complications de FA
= Age élevé / Démence / Saignement récent / Insuffisance rénale terminale / Insuffisance hépatique / Cancer…
– Chez patient ayant saigné récemment :
o Contrôle pathologie causale du saignement
o Réintroduction de l’anticoagulation dès que possible
▪ Choisir les AOD (diminution risque hémorragique digestif) – Voir grande section suivante
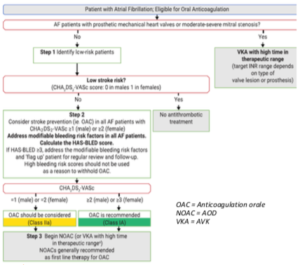
Stratégie d’anticoagulation globale
1. Identifier patients n’ayant pas besoin d’anticoagulants
2. Anticoagulation chez patients avec
≥ 1 FdR non genré d’AVC
3. Choix de l’anticoagulant
-
- – AOD : En 1ère intention
- – AVK : si temps passé dans l’index thérapeutique > 70%
⇒ Recommandations
– R4 : Chez les patients éligibleso Préférer les AOD aux AVK (sauf si prothèse valvulaire mécaniques ou rétrécissement mitral)
o Utiliser le CHA2DS2-VASc
▪ Patient à ne pas anticoaguler
= Score ≤ 0 (ou ≤ 1 chez ♀)
▪ Patient où l’anticoagulation est à discuter
= Score à 1 (ou 2 chez ♀)
▪ Patient où l’anticoagulation est recommandée
= Score ≥ 2 (ou ≥ 3 chez ♀)
– R5 : Evaluer le risque hémorragique par score
o Score HAS-BLED : Score ≥ 3 doit faire augmenter le suivi o Mais risque hémorragique élevé ne doit pas faire éviter les anticoagulants (hors contre-indications)
– R6 : Chez patient à faible risque AVC ⇒ 1er suivi à 4 – 6 mois
– R7 : Stratégie d’anticoagulation
o AVK : Cible d’INR entre 2–3 sur≥70% du temps de prise
o Si pas d’atteinte de la cible ⇒
▪ Education thérapeutique
▪ Relais par AOD
o Eviter la mono/bithérapie par anti-agrégants plaquettaires– R8 : Indication à la fermeture de l’auricule
o Contre-Indication aux AOD/AVK
o Chirurgie cardiaque pour autre cause (fermeture lors de la chirurgie)
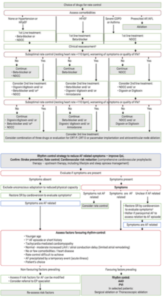
Better symptom management ⇒ Contrôle du rythme / fréquence
Contrôle de la fréquence (Ralentir)
- – Peut suffire à diminuer les sympto
- – Peu d’études de supériorité d’une des stratégies par rapport aux autres
- – Indications de ralentissement de la FA
o Patients asymto / peu sympto de leur FA
o Echec d’une réduction de la FA
(ou risque de complication de la réduction de FA)
– Objectif de contrôle =
o Pour la plupart : FC < 110 bpm
(Etude RACE / AFFIRM : Pas de différence entre < 80 bpm et < 110 bpm)
o Chez patients à FEVG altérée ou avec resynchro bi ventriculaire ▪ Objectif = FC < 80 bpm
▪ En ciblant une FC à l’effort < 110 bpm à 25% du temps de l’épreuve d’effort
▪ Si pacemaker : Vérifier pdt l’épreuve d’effort que le VD/VG sont synchro
▪ Surveillance patient pdt 24h par holter ECG
⇒ Si échec de contrôle (sympto / ↘ FEVG / perte synchro
→ Réduction FA / Ablation NAV
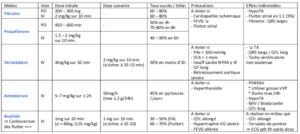
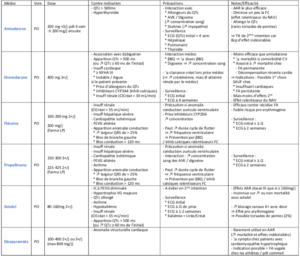
Médicaments disponibles
(PS : Certains anti arythmiques sont ralentisseurs comme l’amiodarone ou le sotalol)
– β bloquants ⇒ Ttt de 1ère intention dans la plupart des cas
– Inhibiteurs calciques non dihydropyridine = Verapamil / Diltiazem
– Digoxine
o Associé à plus forte mortalité
mais biaisé car mis chez les patients les plus graves
o Essai en cours sur patients avec IC à FEVG altéré
– Amiodarone = Traitement médical de dernier recours
o Chez patients non contrôlés par association + CI à ablation du NAV avec pacemaker
o Mais nombreux effets indésirables
Ablation du NAV + Pacemaker [PM]
– Procédure simple
o Implantation PM qq semaines avant ablation NAV
o PM réglé à 70 – 90 bpm, modes de stimulation (VD/biventriculaire) selon le patient
o Etude en cours sur la stimulation du faisceau de His
- – Faible complications/mortalité
- – Ne diminue pas la FEVG voire parfois l’augmente
- – Indications : Echec d’un ralentissement médicamenteux ET
o Patients âgés avec espérance de vie limitée +++
o FA permanente et fortement symptomatique qui ont été hospitalisés ≥ 1 fois pour insuffisance cardiaque
o Chez les patients jeunes : Seulement en urgence (et échec des autres thérapies)
Ralentissement lors d’un épisode aigu
- – Recherche d’une cause (anémie / infection …)
- – Utilisation de βBQ/inhib calciques en 1ère intentiono Objectif : FC < 110 bpmo Utiliser bithérapie si besoin
- – Indication de l’amiodarone IV
o FEVG fortement altérée
o Patient en soins critiques.
(et considérer la cardioversion en urgence)
⇒ Recommandations
– R9 : Contrôle de la fréquence chez
o FEVG > 40% : Utiliser βBQ / Inhib calciques ↘FC o : FEVG < 40% Utiliser βBQ / Digoxine
⇒ Objectif : FC < 110 bpm
– R10 : Possibilité d’une association si échec monothérapie
– R11 : Indications de l’amiodarone IV pour ralentir en aigu
o Instabilité hémodynamique
o FEVG fortement altérée
– R12 : Indications ablation du nœud atrio ventriculaire
o Echec d’une réduction ET ralentissement de la FA et qui ne sont pas éligibles à une ablation dans l’OG et dont le pacemaker est une alternative viable
HFpEF = IC à FEVG préservée / HFrEF = IC à FEVG altérée COPD = BPCO / AF/AFL = FA ou flutter atrial
NDCC = Inhib calciques
CRT-P/D = Resynchronisation cardiaque
Contrôle du rythme (Réduction)
– Réduction = Restaurer rythme sinusal
– Objectifs =
o Réduction des sympto liés à la FA
o Déterminer si sympto sont liés à la FA ou non
– Réduction FA limite passage d’une FA paroxystique en FA persistante
o Etudes en cours sur : Est-ce que la réduction rapide d’une FA nouvellement installée prévient les modifications histopathologiques liées à la FA ?
▪ Chez certains, ça ne semble pas marcher
▪ Essai EAST (2020) ⇒ Diminution des complications liées à la FA lors d’un contrôle précoce de la FA
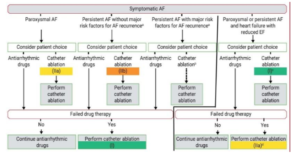
– Indications:
Cardioversion en urgence
– Indication
o En urgence (instabilité hémodynamique) +++
o Mais possible sans urgence vitale
- – Méthode =
o Instabilité hémodynamique
⇒ Choc électrique externe (rapide et efficace)
o Patient stable ⇒ Au choix du patient
▪ Pharmaco : Pas besoin de sédation
▪ CEE : Plus efficace
– Pour les patients stables avec FA paroxystique,
délai de cardioversion <48h avec ralentissement FA entre temps est non inférieur à cardioversion immédiate
Cardioversion à distance (elective cardioversion)
– ⚠ Contre-indication si thrombus vu dans l’OG
o Evaluer risque thrombo embolique
o Considérer utilisation d’anticoagulants oraux ++
(cf. schéma)
– Cardioversion semble améliorer la qualité de vie si maintien du rythme sinusal
– Facteurs de risque de récurrence FA post cardioversion
o Âge élevé
o Sexe féminin
o 1er échec d’une cardioversion o BPCO / Insuffisance rénale
o Cardiopathie structurelle
o OG dilatée
o Insuffisance cardiaque
⇒ Traiter les FdR de récurrence de FA avant cardioversion +++
⇒ Si récurrence de FA → Nouvelle cardioversion précoce +++
Réduction par CEE (urgente ou pas)
- – Réalisé sous sédation (Midazolam/propofol/Ethomidate)
- – Surveillance scopée sur la PA et la SpO2
o Avoir de l’atropine / Isoprénaline pas loin ou avoir la stimulation cardiaque externe
o Utiliser un défibrillateur biphasique
▪ Position électrodes antéro postérieure (efficacité ?)
▪ Choc à énergie max d’emblée
– ± prémédication par AAR qui améliore le succès
– Complications
o Brûlures cutanées
o Bradycardie post CEE
Suivi post cardioversion
– Objectifs du suivi
o ECG post cardioversion pour chercher récurrences
o Efficacité ? sur sympto
o Patient sous AAR classe I ou III : Evaluation PR/QRS et QTc (risque pro arythmogène)
o Recherche des effets indésirables des AAR
o Correction des facteurs de risque de récurrence de FA
Réduction pharmacologique
– 75 – 80% d’efficacité si faite < 48h post hospitalisation
o Surtout sur les FA d’apparition récente
– Possibilité de se laisser 24h (réduction spontanée)
– Médocs possibles
o AAR classe Ic = Flécaine/Propafénone
→ Effet rapide et important
→ Mais possible que si pas d’HVG ou de ↘ FEVG ou ATCD de cardiopathie ischémique
o Amiodarone → Effet lent et peu efficace → Utilisé si FEVG basse
o Vernakalant IV →
▪ Effet très rapide et plus efficace que les 2 autres
▪ Utilisable si ↘ FEVG modérée ou ATCD ischémiques
o Ibutilide → Conversion flutter en rythme sinusal
– Chez patients ayant rares épisodes de FA paroxystiques
→ Dose unique de flécaine chez soi possible
o Efficacité légèrement plus faible qu’en hospitalier
o Mais possible si cardioversion par flécaine a déjà marché en milieu hospitalier sans complications
– Si prise de flécaine ⇒ Ajouter un bloqueur du NAV (risque de flutter 1:1)
⇒ Recommandations
- – R13 : En cardioversion pharmaco ⇒o Préférer vernalakant / flécaine ou propaférone si ∅ CIo Sinon amiodarone IV
- – R13.b : La cardioversion pharmaco ne se fait que chez patients stables (et en tenant compte du risque embolique)
- – R14 : Une prémédication par AAR (ceux de la cardioversion pharmaco) peut être réalisée avant cardioversion électrique pour ↗ succès
- – R15 : Tout patient avec FA persistante symptomatique doit être cardioversé
- – R16 : Patients qui ont une FA paroxystique déjà réduite par AAR classe Ic peuvent prendre une dose unique PO chez eux en cas de récurrence de FA
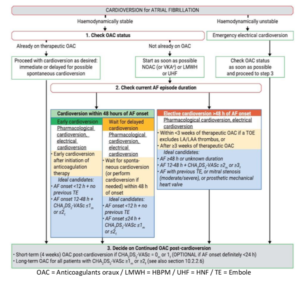
Gestion du risque d’AVC pendant la cardioversion
- – ↗ risque d’AVC/embolie si FA ≥ 12h sans anticoagulationo 0,1% si FA ≤ 12h et risque faible d’AVC (CHA2DS2VASc ≤ 0 (♂)/≤ 1 (♀))
- – Mécanismes liés à ↗ risque embolique lors cardioversiono Présence initiale d’un thrombus
o Changement mécanique atriale lors retour rythme sinusal o Paralysie post cardioversion
o Etat post thrombotique - – ∅ essai comparant anticoagulation vs. ∅ anticoagulation sur les FA apparues ≤ 48h
- – Stratégie d’anticoagulation PRE cardioversion
o AVK trop lents pour atteinte cible INR
o Recherche thrombus par ETO
▪ Si ∅ thrombus ⇒ Cardioversion sous héparine ⇒ Anticoagulation orale au décours
▪ Si ∃ thrombus ⇒ Anticoagulation pendant 3 semaines ⇒ Nouvelle ETO avant cardioversion
o AOD +++ = 3 semaines avant cardioversion
▪ Aussi efficaces que les AVK (voire même plus efficace)
- – Stratégie anticoagulation POST cardioversion
o Anticoagulation selon risque AVC (CHA2DS2VASc) et risque hémorragique (cardioversion réussie ne doit pas éviter l’anticoagulation si le risque d’AVC est élevé)
⇒ Recommandations
– R18 : Anticoagulation par AOD lors cardioversion (aussi efficace / sûr que les AVK)
o Durée = 3 semaines avant cardioversion
o Si ∅ anticoagulation ⇒ Vérifier par ETO pour exclure le thrombus▪ Si présence d’un thrombus : Anticoagulation pdt 3 semaines +++
▪ Contrôle ETO après anticoagulation avant cardioversion
– R19 : FA cardioversée apparue < 48h = Cardioversion possible sansobligation de recherche thrombus par ETO
– R20 : FA cardioversée apparue > 24h = Anticoaguler tout patiento Durée : 4 semaines au moins ∀ résultat cardioversion
o Si risque d’AVC (CHA2DS2VASc) ⇒ Continuer anticoagulation
– R21 : FA cardioversée apparue ≤ 24h
ET Faible risque AVC (CHA2DS2VASc ≤ 0 (♂)/≤ 1 (♀))
⇒ Possible d’éviter l’anticoagulation post cardioversion
Ablation de la FA par cathéter
– Plus efficace que les AAR au long cours
Pour maintien rythme sinusal et ↗ qualité de vie
o En 1ère intention ou après échec des AAR
o Mais peut nécessiter plusieurs gestes si récidive
o Mais ∅ essai sur la réduction des AVC
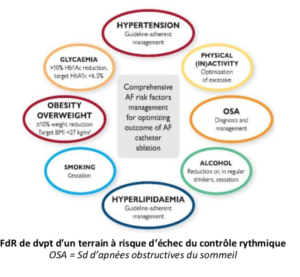
⇒ Nécessité d’un contrôle des FdR d’échec (cf. figuree)
– Indications d’ablation FA par cathéter
o Choix du patient +++
o FA chez insuffisant cardiaque ↘ FEVG naïf d’un ttt AAR
o Echec des AAR dans une FA paroxystique/permanente sans ↘ FEVG
o Cardiopathie rythmique sur FA dont la FEVG est +/- restaurée après correction arythmie
– Pas d’indication d’ablation de FA chez asymptomatique
 Techniques d’ablation de FA par cathéter
Techniques d’ablation de FA par cathéter
- Isolation des veines pulmonaires par lésions autour de leur orifice –
o Par utilisation de sondes radiofréquences (RF) ou d’appareil en un coup. o Isolation difficile (reconnection possible dans 70% cas)
o Si FA persistante : Autres techniques en cours d’étude
▪ Extension ablation sur OG / auricule gauche / VCS ▪ Ciblé par IRM
▪ Ablation des sites majeurs d’arythmie
o Si patient avec flutter sur isthme cavo tricuspide ⇒ Ablation isthme droit
- Ablation au cryoballon
o Aussi efficace que vs. Radio fréquence sur une FA paroxystique (mais ptet plus faibles complications au ballon)
o Plus efficace que les AAR seuls sur une FA paroxystique
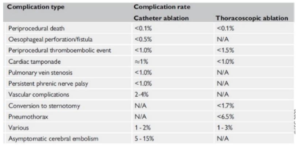
Complications = 5 – 15% des cas (parmi lesquels 2,5% sont fatals)
- – Apparaissent dans les 24h en général (± qq mois après)
- – Risque de récidive de FA post ablationo Multiples facteurs (âge / taille OG / durée de FA / ↘ FEVG / Insuff rénale…) o Predicteur puissant = Récurrence proche de la FA
Modalités de suivi post ablation par cathéter
-
- – Informations des risques
- – Monitorage par ECG/Holter/smartphone
o A 3 mois puis 1×/an
o Récurrence au dela 1 mois ⇒ Prédisent des récurrences
→ Mais possible FA asymptomatique
- Anti arythmiques (AAR)
o Poursuite possible des AAR pdt 6 sem – 3 mois (peut ↘ récurrences …)
o Après ∅ reco (Arrêt / continuer selon les sympto / récidive)
-
- – Anti coagulation post ablation
o A continuer pendant 2 mois ∀ patient ablaté
o ≥ 2 mois post ablation : Anticoagulation selon le CHA2DS2VASc
⇒ Recommandations
- – R22 : Indication ablation par isolation V. pulmonaires
o Echec / intolérance des AAR de classe I ou III chez patients en FA paroxystique ou persistante
o A considérer chez patients avec échec des βBQ
- – R23 : Chez patient dont l’isolation des V. pulm a déjà marché⇒ Si récurrence : Possibilité de répéter le même geste
- – R24 : Contrôle strict des FdR et déclencheurs de récidive de FA ++
- – R25 : Les technique recommandées sont
o ∀ patient = Isolation des veines pulmonaires o Lésion isthme cavo tricuspide chez▪ Flutter atrial induit lors par ablation FA
▪ Flutter sur isthme cavo tricuspide
Gestion du risque d’AVC lors d’une ablation par cathéter
– Réalisation du geste sous AVK/AOD (sans interruption)
o Préférer les AOD aux AVK (efficacité similaire, mais moins d’hémorragies)
o Eviter le relais héparine (↗ risque hémorragique)
⇒ Recommandations
- – R26 : Chez patients à risque d’AVC (CHA2DS2VASc ≥ 1 (♂)/≥ 2 (♀)) –⇒ Stratégie d’anticoagulation par
o AOD/AVK pendant au moins 3 sem avant o ETO pour exclure un thrombus - – R27 : Chez patients déjà sous AVK/AOD à dose curative ⇒ Réaliser l’ablation sous anticoagulation
- – R28 : Anticoagulation post geste
o AOD/AVK systématique pdt 2 mois
o Au-delà de 2 mois : Anticoagulation selon le risque d’AVC
Chirurgie de la FA
– Efficacité de la chirurgie
o Efficacité démontrée sur arrêt de l’arythmie
o Mais efficacité peu connue sur la survie / qualité de vie … (mais retrouvée vue sur des registres)
– Chirurgie FA combinée à une autre chirurgie cardiaque
Coopération entre chir cardiaques et électro physiologistes
▪ Technique du « Cut and sew maze » =
• Isolation veines pulmonaires + mur postérieur de OG
(pas de l’OD) par lignes d’ablation en labyrinthe
par pince bipolaire / cryothérapie (lésion voies de conduction) ⇒ ↕ influx aux valves mitrales/tricuspides et veine caves
⇒ Exclusion de l’auricule gauche
▪ Chez patients en FA permanente : Ablation sur l’OD et l’OG
Ablation de FA lors d’une chirurgie = ↗ risque de besoin d’un pacemaker
– Chirurgie FA seule
o Chirurgies possibles
▪ Ablation par RF en thoracoscopie
⇒ Cible V. pulmonaires / Mur postérieur OG
▪ Fermeture de l’auricule
⇒ Que chez patients sans anomalie cardio structurelle
o Efficacité : Ablation en thoracoscopie meilleure que l’ablation par cathéter (étude FAST)
▪ Mais ↗ durée hospitalisation + complications (4-10%)
▪ Poursuite de l’anticoagulation selon le CHA2DS2VASc (∅ preuve efficacité sur AVC)
o Indication : Echec d’une ablation cathéter ou risque d’échec
Ablation hybride de la FA par cathéter + chirurgie
= Approche minimaliste épicardique invasive (sans sternotomie) + Cathéter en endocardique
- – En 1 temps ou séquentiel (ablation KT dans les 6 mois si récidive) → ∅ étude comparant les 2 stratégies
- – Efficacité supérieure à l’ablation par KT seule (∀ prise AAR) Mais plus de complications
Gestion du risque d’AVC sur une chirurgie de FA
– Anticoagulation ∀ patients en post op
o Méca : Lésions endothéliales en post op
o Dès que possible
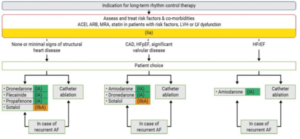
Anti arythmique longue durée après réduction FA
- – Objectif des AAR longue durée = Améliorer les sympto de la FA
- – Choisir l’AAR selon la tolérance (et pas l’efficacité)o Effets 2nd fréquents ++ (dont pro arythmogène ++)
- – Efficacitéo ↗ maintien en rythme sinusal (mais n’élimine pas le risque)o AAR possibles après 1er échec AAR et ablation FA
- – Echec d’un AAR ⇒ Changer pour un autre AAR
- – Durée courte des AAR ?
o Ne prévient pas contre les récurrences tardives (que des récurrences précoces)
o ↘ effets indésirables
o Indications :
▪ Risque d’effets 2nd des AAR
▪ Risque faible de récurrence de FA
– Règles de traitement par AAR
o Quand initier ? ⇒
▪ Patient sympto ? (score EHRA)
▪ Pas dès la 1ère crise (mais ↗ efficacité cardioversion)
o Quel AAR utiliser ? ⇒ Choix selon
▪ Anomalie ECG initiale (QRS long / PR long / QTc allongé)
▪ Impact sur fonction VG
▪ Interaction avec autres médocs
o Comment éviter effet pro arythmogène ?
- ▪ ECG pendant le traitement(± Holter/Epreuve d’effort chez certains)
- ▪ Eviter combinaison d’AAR
- ▪ Rechercher les toxicités d’organes
o Comment évaluer efficacité ?
▪ Demander au patient nb d’épisodes de FA ▪ Si AAR efficace mais arrêté car intolérance
⇒ Reprise d’un AAR différent de même classe o Cas particuliers
▪ Ablation FA ⇒ Possible durée courte d’AAR seule
▪ Patients avec anomalie conduction AV/dysfonction sinusale
⇒ Discuter du pacemaker si nécessité d’AAR
⇒ Recommandations
- – R29 : Chez patients devant subir une chir cardiaque, discuterablation FA
- – R30 : Indications de la chirurgie de la FA isolée (ou hybride)o FA symptomatique réfractaire aux AAR et ablation cathéter o Risques évidents d’échec d’ablation par cathéter
o A discuter chez FA persistante à risque de récurrence+ et échec ≥ 1 AAR, dont le patient souhaite l’ablation⇒ A évaluer en équipe chir + électro physiologistes - – R31 : Anticoagulation au long cours que selon le risque d’AVC
- Médocs non AAR à propriétés anti arythmiques (en dvpt)
o FA est fortement associé à cardiopathie atriale
⇒ Modification remodelage atrial peut diminuer FA
o Etude RACE3 = Contrôle des FdR de FA aide au contrôle de la FA
o Médocs en cours d’étude
▪ IEC / ARA 2 : A poursuivre si anomalie structurelle cardio
↗ activité SRAA en FA
Efficacité non prouvée dans les essais (surtout chez ceux qui n’ont pas d’anomalie structurelle)
▪ Anti-aldostérone :
Aldostérone impliquée dans initiation/pousuite de la FA
Peut être efficace pour éviter FA chez les IC ∀ FEVG (mais amélioration IC diminue risque de FA donc …)
▪ βBQ hors sotalol : Non efficace pour retour rythme sinusal
▪ Statines : Essai = ∅ efficacité sur FA / prévention FA
Risque pro arythmogène des AAR
- – FdR ↗ risque pro arythmogèneo Âge avancé
o Sexe féminin
o Insuff rénale/hépatique
o Utilisation d’AAR
o Hypokaliémie
o ATCD fam de mort subite
o Cardiopathie ischémique
o Hypertrophie VG
o FEVG altérée
o PR allongé / QRS allongé / QTc allongé - – Survenue des évènements pro arythmiques
o Au début du ttt, surtout si dose de charge
o Quinidine : Indépendant de la dose
o Sotalol : Pro arythmogène même si ∅ anomalie cardiaque
⇒ Recommandations
– R32 : Amiodarone est recommandé ∀ patients avec FA Mais considérer autres AAR du fait de sa toxicité– R33 : Dromédarone est indiqué en AAR longue durée chez
o FEVG normale ou légèrement altérée (mais stable) o IC à FEVG préservée
o Cardiopathie ischémique
o Pathologie valvulaire– R34 : Flécaine/Propafénone
o Indiqué chez FEVG normale + ∅ anomalie cardiaque structurelle (∅ ischémie / ∅ hypertrophie VG)
o Discuter d’un médoc bloqueur du NAV– R35 : Sotalol à discuter chez o FEVG normale
o Cardiopathie ischémique ⇒ Surveillance +++– R36 : Eviter les AAR chez
o FA permanente avec ralentissement FCo Troubles conduction AV non appareillés
Cardiovascular comorbidities optimization ⇒ Contrôle des FdRCV
- – FdRCV et comorbidités contribuent au remodelage atrial ⇒ FA
- – Contrôle des FdRCV permettento ↘ risque d’AVCo ↘ durée de FA et des symptômes
- – Nécessite un contrôle global (un seul FdRCV ne suffit pas)Mesures sur le mode de vie
- – Obésité
o ↗ risque FA / AVC avec l’IMC
o ↗ complications / irradiation lors ablation
o ↗ risque récurrence post ablation (± SAOS)
⇒ Mais ne contre indique pas l’ablation FA chez les obèses - – Consommation d’alcool
o ↗ risque FA et saignement sous anticoagulants
(faible adhérence, maladie hépato, ↗ risque trauma) o ↗ risque thrombo embolique
- – Consommation de café = ∅ lien avec FA
o Peut être associé à ↘ risque FA
o Mais ↗ sympto (palpitaion) sans lien avec FA - – Activité physique
o ↗ risque FA chez les sportifs (surtout en endurance) o Recommandations chez patient FA
▪ Exercice physique modéré
▪ Eviter exercices d’endurance prolongés (marathons …)
(surtout si ≥ 50 ans)
⇒ Recommandations
- – R37 : Identifier et traiter tous les FdR/comorbidités
- – R38 : Chez patients HTA : Dépistage ciblé de la FA recommandé
- – R39 : Patients HTA + FA ⇒ Contrôle strict TA
(↘ risque AVC/saignement et ↗ contrôle FA)
- – R40 : Patients obèses ⇒ Perte de poids
- – R41 : Patients alcooliques ⇒ Infos + Sevrage, surtout pouro Prévention d’apparition de FAo ↘ risque saignement sous anticoagulants
- – R42 : Poursuite d’une activité physique modéréeo En évitant si possible les exercices d’endurance prolongée
- – R43 : Patient avec SAOSo Dépistage ciblé FA possible
o Traiter le SAOS peut ↘ FA (apparition/sympto …)
Mesures cardiovasculaires
- – HTA → 1er FdRCV retrouvé dans la FAo ↗ risque de FA chez un HTA
o ↗ risque AVC/saignement sous anticoagulants lors HTA o Recommandations▪ Ttt anti HTA strict avec objectifs TA ≤ 130/80
▪ Considérer patient HTA chronique / non contrôlé comme àhaut risque d’AVC
▪ Ne pas utiliser de sotalol si- Cardiopathie HTA avec HVG
- Insuffisance rénale
▪ Correction des autres FdR d’HTA (SAOS / Alcool / Obésité)
- – Insuffisance cardiaque / Cardiopathie ischémique⇒ Cf. partie suivante
- – Diabétiqueo ↗ risque de FA chez les jeunes
▪ Surtout asymptomatiques (neuropathie)
▪ ↗ risque avec ↗ complications micro vasculaireso ↗ risque d’AVC (diabétique type 1 ou 2)
o Contrôle glycémique n’affecte pas le taux de nouvelles FA▪ Mais possible effet methformine et pioglitazone pour ↘ FA à long terme▪ Par contre, ↘ récurrence de FA si ablation FA
o ∅ interaction entre diabète et anticoagulants oraux - – Apnée du sommeil
o Forte prévalence parmi patients en FA / HTA / IC o Mécanismes SAOS entrainant la FA▪ Hypoxémie / Hypercapnie
▪ Modification pressions intra thoraciques
▪ Déséquilibre sympathique / parasympathique ▪ Stress oxydatif + inflammationo SAOS ↘ réussite de toutes les modalités de réduction de FA o Ttt SAOS par PPC/VNI augmente le taux de réduction de FA o Recommandations▪ Recherche d’un SAOS avant réduction d’une FA
▪ Mais si ∅ réduction : ∅ reco sur recherche/ttt d’un SAOS
Prise en charge de la FA dans des situations particulières
Instabilité hémodynamique
- – Instabilité hmd sur FA = FC élevée associée à … o Syncope / ↘TA sympto
o Choc cardiogénique
o Infarctus myocardeo OAP - – Contrôle rythme chez ces patients est difficileo Inotropes / vasopresseurs ⇒ ↗ FA
o Activation sympathique endogène ⇒ ↗ FA o FEVG altérée - – Médoc de choix pour ralentir = βBQ (> digoxine)
o Digoxine ne marche pas du fait de l’activation sympathique o Inhib calciques contre indiqués si ↘ FEVG
o Amiodarone IV possible, risque d’↘ TA
FA et cardiopathie ischémique (aigu/chronique)
– Chez patients avec SCA : ↗ risque FA (de 60%) o Anticoagulation non optimale
o ↗ effets indésirables
- – FA associé à SCA ST+ ou sans élévation du ST.
- – Stratégie post coronarographie
o En général : Clopidogrel seul + AOD (> AVK) ▪ ↘ risque hémorragique vs. Trithérapie
▪ Pour un risque embolique équivalent
o Mais ceux à risque embolique élevé peuvent bénéficier d’une trithérapie courte
(2 AAP [anti agrégant plaquettaire] + AOD)
– Ticagrelor/Prasugrel ⇒ ↗ risque hémorragique ⇒ A éviter donc +++
⇒ Recommandations =
– R44 : CEE en urgence chez patients en FA avec instabilité hmdo Possibilité d’utiliser l’amiodarone pour ralentir
1er diagnostic de FA chez patient
- – Diagnostic à préciser sur la durée (type de FA …) ⇒ Non classée
- – Pronostico Faible prescription d’anticoagulant chez ces patients
o Mais registres montrent un pronostic moins favorable queFA paroxystique (≈ pronostic FA permanente)
⇒ Suivre le pattern A.B.C du traitement de la FA chez ces patients +++Durées de ttt
o Association Clopidogrel + anticoagulant pendant▪ SCA ST+/- : 12 mois▪ Angor chronique : 5 mois o Puis : anticoagulant seul▪ ∀ type stent, tant qu’il y’a pas eu thrombose)
▪ Pareil si cardiopathie ischémique sans coronarographie Patient à risque d’ulcère gastro duodénal ⇒ Couverture par IPP Patient traité par pontage coronaire ⇒ Clopidogrel + AOD/AVK
– Contrôle +++ de la fréquence cardio
o βBQ ou inhib calcique
o Cardioversion si instabilité hémodynamique o ⚠ Contre-indication à
▪ Vernakalant
▪ Flécaine / Propafénone – Contrôle ++ des FdRCV
⇒ Recommandations
– R45 : Si anticoagulation indiquée⇒ Préférer les AVK aux AOD en général o Si risque hémorragique HAS-BLED ≥ 3
⇒ Préférer
▪ Rivaroxaban 15mg/j (↘ dose)
▪ Dabigatran 110 mg 2×/j (↘ dose)o Cible INR : 2 – 2,5 (avec temps dans INR > 70%) – R46 : Si coronarographie sans complications
+ autre facteur parmi :
o Risque thrombose de stent faible
o Risque hémorragique plus grave querisque thrombose stent
⇒ Aspirine + Clopidogrel + Anticoagulant pdt 1 semaine
⇒ Puis Clopidogrel seul + anticoagulant pdt▪ 12 mois si SCA ST +/-
▪ 6 mois si angor chronique
- – R47 : Si risque thrombose stent plus grave que risque hémorragique⇒ Triple thérapie pendant ≤ 1 mois avec o Aspirine + Clopidogrel
o Anticoagulant oral- – FdR de thrombose de stent chez angor chronique o Stent du tronc commun gauche
o Déploiement stent non optimaal
o Longueur stent > 6 cmo Double stent sur bifurcation
o Traitement occlusion totale
o ATCD de thrombose de stent sous AAP o Diabète
o Insuff rénale aigue
AVC ischémique / Hémorragie intra crânienne chez patient en FA AVC ischémique / AIT
– AVC sur FA est souvent fatal
o Risque de récurrence entre 48h – 2 semaines
o Risque de transformation hémorragique dans les 1er jours
(thrombolyse + lésions embolique)
- – AVC peut induire de la FA ≈ Lésion insula
- – Prévention des récidives d’AVC
o Pas de timing précis de reprise de l’anticoagulation ▪ Eviter toute anticoagulation dans ≤ 48h
(↗ hémorragie sans ↘ risque récidive AVC)
▪ Mais délai reprise anticoagulation en cours d’essai ++
o Pt de vue cardio : Reprise dès que possible ⇒ Avis multidiscipliaire
o Optimiser la reprise de l’anticoagulation
▪ AVK : Si INR impossible à atteindre ⇒ Relais AOD ▪ AOD : S’assurer de la bonne dose +++
(↘ dose fait ↗ risque AVC sans ↘ risque hémorragique)
o AOD > AVK pour ↘ risque récidive AVC et ↘ risque hémorragique o Inutilité de
▪ Ajouter aspirine au traitement anti coagulant ▪ Augmenter la cible d’INR
– AVC chez patient sous anticoagulants
o Eviter la thrombolyse si anticoagulation continue o Patient sous AVK : Thrombolyse possible si
▪ INR < 1,7
▪ Exclusion de l’hémorragie par imagerie cérébrale o Patient sous AOD
- ▪ TCA (dabigatran) / Anti Xa (-xabans)
- ▪ Heure de dernière prise AOD(≥ 48h = sûr en général)
- ▪ Possible réversion du dabigatran par idarucizumab⇒ Recommandations
– R48 : Chez patient FA avec un AVC ischémique / AITo Anticoagulation à long terme si ∅ CIo Préférer les AOD aux AVK
– R49 : ⚠ En aigu, pas d’anticoagulation (héparine / AVK / AOD)dans les 48h premières heures de l’AVC +++
AVC cryptogénique
– Pas d’anticoagulation si
o Si AVC ischémique sans étiologie précise –
o AVC embolique sans FA associée
– Essais en cours sur certains sous groupes qui pourraient en profiter o Age ≥ 75 ans
o OG dilaté
o Insuffisance rénale
Améliorer détection de la FA chez ces patients o Score prédisant « haut risque de FA » C2HEST
▪ Cardiopathie ischémique / BPCO = 1 pt chaque ▪ HTA = 1 pt
▪ Ederly ≥ 75 ans = 2 pts
▪ Insuff cardio systolique = 2 pts
▪ Hyperthyroïdie = 1 pt
o ECG réguliers ± holters ⇒ ↗ sensibilité détection FA
(mais effet inconnu sur mortalité car ∅ essai clinique)
⇒ Recommandations
R50 : Chez patients avec AVC / AIT sans FA connue o ECG sur 24h minimum
o Puis si possible holter ECG sur 72h– R51 : Indications à holter ≥ 72h ou holter implantable chez patient sans FA
o Patient âgé / FdRCV / Signes de remodelage OG= Score C2HEST élevé
o AVC/AIT cryptogénique d’allure embolique
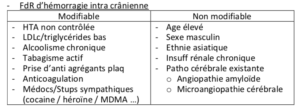
Hémorragie intracrânienne
– Peur de réintroduire des anticoagulants après hémorragie o Mais nécessaire si patient FA (à risque d’AVC)
o A faire en décision collégiale +++
(neurochir, neurologues, cardiologues, patients) o ± s’aider d’une imagerie cérébrale
– Peu d’essais anticoagulants + FA chez ces patients o Patients qui sont souvent exclus
(par leur ATCD d’hémorragie cérébrale récente) o Mais preuves observationelles suggère
qu’ils pourraient en bénéficier
– Comparaison AOD/AVK sur les hémorragies cérébrales o AOD moins à risque de saignement que les AVK
(mais si saignement, survie/taille saignement identique)
o ∅ essai clinique ⇒ Mais recommandation des AOD chez les patients avec ATCD d’hémorragie cérébrale
– Stratégie d’anticoagulation
o Considérer les facteurs suivants
▪ Hémorragie non traitable / irréversible
▪ Hémorragie lors arrêt anticoagulation
▪ Hémorragie sur anticoagulation bien ou sous dosée ▪ Nécessité d’une anti agrégation plaquettaire
Tenir compte des micro bleeds cérébraux
o Présence de micro bleeds ⇒ ↗ risque hémorragique
o Mais si ATCD AVC sur FA ⇒ Risque d’AVC ischémique est plus élevé que le risque d’hémorragie intra crânienne
⇒ Recommandations
– R52 : Chez patients en FA à haut risque d’AVC, après hémorragie intracrânienne sur trauma / spontanée
o Concertation multidisciplinaire avec les neuroo Préférer les AOD aux AVK si possible
Hémorragie active sous anticoagulation
- – 1. Compression des sites hémorragiques si possible
- – 2. Evaluation
o Hémodynamique o Hémostase
▪ AVK ⇒ INR ▪ AOD ⇒
- Dabigatran = Temps de thrombine / Temps reptilase (ou Ecarin)
- -Xabans = Anti Xa
o NFS + Num plaquettaire o Fonction rénale
– 3. Dernière prise d’anticoagulants ?
FA et insuffisance cardiaque
- – Coexistence ↗ risque décès des 2 patho
- – Effets AOD non changés si insuff cardio
- – Cependant, contrôle fréquence plus difficile
o Objectif FC ≤ 110 bpm o Médocs utilisables
▪ FEVG N : βBQ / Inhib calciques / Digoxine
▪ FEVG ↘ : βBQ / Digoxine
▪ Amiodarone, mais que pour contrôle rythme en aigu ++
o Si échec : Ablation du NAV + Pacemaker
– Réduction de la FA ?
o Etude observationnelle = ↘ mortalité si FEVG N
o Si instabilité hémodynamique / Aggravation IC
⇒ Réduction de la FA (CEE en urgence / Amiodarone sinon)
o Ablation FA au cathéter
⇒ Efficace pour ↘ sympto/mortalité
FA et pathologie valvulaire
- – Patho valvulaire est associé à la FA(1/3 des patients FA ont une patho valvulaire)
- – FA = ↘ pronostic chez patients valvulopathe sévèreo ↗ risque embolique et AVC (∀ valvulopathie)
- – Preuves contradictoires sur les AOD danso Les patho rhumatismales mitrales
o Les 3 premiers mois après implantation d’une bioprothèse
(arrêt RCT chez patient non en FA car AOD ↗ mortalité et saignement)FA et Insuffisance rénale chronique
- – Insuff rénale est une patho pro thrombotique et pro hémorragique
- – Lien entre FA et insuff rénaleo FA présent chez 20% des insuffisants rénaux
o 50% des patients ont une insuff rénale
o ↘ fonction rénale ⇒ Prédicteur de risque thrombose/hémorragie - – Anticoagulation et insuffisance rénale
o IR modérée (30 – 50 mL/min de ClCreat) = Pas d’altérationefficacité ou sécurité des AOD par rapport aux AVKo IR sévère (< 30 mL/min de ClCreat) ⇒ ∅ données (patients souvent exclus des essais)
+ ∅ AMM des AOD dans ce cas⇒ Essais en cours pour AVK/AOD
chez les insuffisants rénaux terminauxFA et pathologie endocrinologiques
- – Patho à risque de FA
o Troubles ioniques
o Glycémies incorrectes
o Dysthyroïdies
o Acromégalie
o Phéochromocytome
o Insuffisance surrénale
o Atteinte parathyroïdes
o Insuffisance pancréatique - – Si FA associée à hyperthyroïdie
o Retour à l’euthyroïdie réduit la FA d’elle-même
o ⚠ Contre-indication à l’amiodarone
o Pas d’ablation de FA cathéter si pas d’euthyroïdie (ni de troubles métaboliques)
FA et pathologie hématologique
– ↗ risque d’hémorragie sous anti coagulants si o Anémie
o Thrombopénie
- ⇒ Correction anémie / thrombopénie avant anticoagulation
- ⇒ Concertation multidisciplinaire avant anticoagulationchez patients ayant < 100G/L de plaquettes
– Certaines chimio sont à risque de
o FA = Ibrutinib, Melphalan, anthracyclines o Thrombopathie (Ibrutinib)
FA chez les personnes âgées fragiles
- – ↗ prévalence FA avec l’âge (et ↗ complications FA avec l’âge)
- – ↘ prescription d’anticoagulants oraux dans cette populationo Malgré preuves évidentes de leur efficacité (nombreux essais) = ↗ faible risque saignement est largement
compensé par ↘ risque d’AVCo Préférer les AOD aux AVK
o Eviter de remplacer ttt standard par▪ Anti agrégants plaquettaires▪ ↘ doses d’AOD - – Stratégie préférée pour ↘ sympto = Ralentir FAo Mais peu de preuves sur les ttt ralentisseurs/réducteurs de FA dans cette population
o Ablation FA au cathéter peut être envisagé chez certaines personnes (mais ↗ âge = ↗ risque complications/récurrences)
⇒ Recommandations
R54 : Indication à anticoagulation par AVK seuls o Rétrécissement mitral ≥ modéré
(mais ptet qu’AOD sont mieux dans ce cas)
(étude observationnelle)
o Prothèse mécanique de valve (⚠ CI des AOD) ⇒ AOD possible pour les autres valvulopathies
FA et artériopathie périphérique
– Association d’un artériopathie chez patient FA fréquente
o ↗ risque d’AVC (surtout si plaque dans l’aorte descendante)
– Recommandations
o Dépistage régulier de la FA chez patients artéritiques
o Anticoagulation orale systématique
o Si artériopathie stable (= ∅ complications si FA vasc sur 1 an)
⇒ Arrêt des anti agrégants et utilisation AOD/AVK seul (Ajout aspirine ne change pas survie, mais ↗ saignement)
– Pour ralentir une FA chez patient artéritique
o βBQ peut aggraver sympto de sténose artérielle
⇒ Remplacer par inhib calcique bradycardisants
FA et saignements gastro intestinaux
– Lien avec les patho digestives
o Lésion digestives ⇒ ↗ risque hémorragie sous anticoagulants o MICI ⇒ ↗ risque AVC et apparition FA
– Hémorragie digestive
o Risque similaire de saignement entre AVK et AOD
o Reprise anticoagulation dès que lésion digestive est traitée
– Dabigatran = Risque de dyspepsie – Hépatopathie chronique
o ↗ risque hémorragique (↘ fct° hépatique / varices …) o ↗ risque thrombotique
o ∅ essais sur ces populations (exclusion fréquente)
▪ Mais pas de problème en particulier si prise d’AOD dans une étude observationelle
▪ Risque hémorragique similaire entre AOD et AVK
⇒ Possibilité d’AOD si hépatopathie aigue ou cirrhose ≤ modérée ⇒ ⚠ Contre-indication des AOD si cirrhose Child C
(et éviter rivaroxaban si cirrhose Child B)
FA chez patients déments
– Anticoagulation peut protéger contre démence
chez patient à risque d’AVC
o Nécessité d’avoir une anticoagulation efficace (INR dans l’objectif pdt ≥ 70% du temps)
o Meilleure efficacité des AOD (mais inconstante) par rapport aux AVK
– Existe un effet protecteur de l’anticoagulation
o Même chez patients n’ayant pas besoin d’être anticoagulés ⇒ Essais en cours sur les AVK/AOD pour prévenir la démence chez les patients FA
– Démence peut modifier observance de ttt ⇒ ↗ complications chez patients FA
– En post ablation de FA par cathéter
⇒ Apparition de micro lésions cérébrales à l’IRM mais sans altération cognitive
FA et anomalies congénitales
- – Peu de données sur la FA chez ces patients
- – Contrôle fréquence à risque de bradycardie et ↘ TA
- – Contrôle rythme possible
o AAR type Ic supprime 50% de l’arythmie atriale (mais effet pro arythmogène à considérer)
o R57 : Si cardioversion ⇒
▪ Anticoagulation 3 semaines
▪ ETO de contrôle à discuter même si anticoagulé
- – Si défaut paroi septale atriale ⇒ Prévention FA
par fermeture du défect avant 40 ans
o Si apparition FA ⇒ Ablation FA par chirurgie/cathéter - – Patient avec fermeture d’un FOP ont ↗ risque de FA
o ⚠ Si FA avec FOP, ne pas faire la fermeture du FOP⇒ Préférer anticoagulation oraleFA dans cardiomyopathies / Tb du rythme congénitales
- – ↗ prévalence de FA dans ces populationso FA peut être même la seule manifestation cliniqueo ↗ complications de la FA
- – Règles
o Certains médocs sont contre-indiqués
▪ QT long congénital = Tous les allongeurs du QT ▪ Brugada = AAR classe I
o FA peut causer des chocs inappropriés si porteur
d’un défibrillateur implantable
▪ Pose d’une sonde atriale si ↘ FC sous βBQ
▪ Réglage : Choc si FV ≥ 210-220 bpm sur longue durée
FA pendant la grossesse
- – Cause fréquente d’arythmie cardiaqueo ↗ Risque de décèso ↗ risque thrombotique (état hyper coagulable)
- – FdR de FA pendant grossesseo Cardiopathie congénitaleo Age maternel élevé
- – Anticoagulation
o Suivre les indications générales (CHA2DS2VASc) o Médocs selon trimestre
▪ T1 : HBPM
▪ T2 : HBPM ou AVK
▪ T3 : HBPM ou AVK (éviter AVK si sténose mitrale significative)
o ⚠ Contre-indication aux AOD pendant la grossesse
o ⚠ Eviter l’accouchement par voie basse sous AVK – Réduction FA préférée ++
o CEE possible si instabilité / risque pour fœtus ▪ Faibles conséquences pour le fœtus
▪ Anticoagulation préalable recommandée ▪ Surveillance du RCF post CEE
o Ibutilide / Flécaine possible si ∅ cardiopathie congénitale
FA chez les athlètes professionnels
- – Activité physique
o Modérée ⇒ ↘ risque de FA
o Intense ⇒ ↗ risque de FA (5 fois) - – Facteurs de risque de FA chez athlètes o Sexe masculin
o Age dans la quarantaine
o Sport d’endurance ⇒ A risque +++ o Taille élevéeo Nombre d’heure de sport > 1500-2000h - – Peu d’essais clinique dans cette population
– Règles
o Eviter les sports de contact si prise anticoagulants o Ttt médicamenteux rarement bien tolérés
▪ Population à risque de bradycardie/pause sinusales
▪ Digoxine/Verapamil ⇒ Rarement efficace
▪ Beta bloquants ⇒ Mal tolérés ± Contre indiqués parfois ▪ Mono dose de flécaine possible
(mais éviter sports tant que :
- FA cesse
- Dépasser 2 demie vies du médoc
o Ablation de FA souvent efficace ++
⇒ Recommandations
– R55 : Patients avec ATCD de FA/Flutter/Tachycardie atriale à ré-entrée+ ≥ 1/4 ATCD parmi
o Chirurgie intra cardiaque
o Cardiopathie cyanogène
o ATCD de chirurgie de Fontan
o VD systémique
⇒ Anticoagulation systématique chez ces patients– R56 : Chirurgie de la FA indiquée si
o ATCD de d’arythmie atriale symptomatique chez patient nécessitantla fermeture d’un défect atrial
o FA symptomatique chez qqn nécessitant une chirurgie cardiaquepour corriger des malformations congénitales
– Patients avec Wolf Parkinson White o Risque de super FA =
▪ Rythme ventriculaire très rapide
par passage influx par voie accessoire
▪ ↗ risque de FV et de mort subite o Règles
- ▪ Cardioversion électrique si instabilité hémodynamique
- ▪ Eviter les ralentisseurs du NAV(Verapamil, βBQ, Digoxine)
- ▪ Cardioversion médicamenteuse
- Préférer l’ibutilide +++
- Eviter AAR classe Ic / Amiodarone ⚠⇒ Recommandations
– R57 : Gestion en aigu
o Instabilité hémodynamique ⇒ CEE en urgence
o Cardiopathie hypertrophique ⇒ Cardioversion à discuter o ∅ anomalie congénitale▪ Cardioversion par Ibutilibe / Flécaine ▪ Si échec des bloqueurs du NAV
⇒ Flécaine / Propafénone / Sotalol – R58 : Gestion en chronique
o Anticoagulation systématique pour patients FA
o Si échec réduction FA ⇒ Contrôle fréquence cardiaque▪ 1ère intention : βBQ (de préférence β1) ▪ 2ème intention : Digoxine / Verapamil
FA post opératoire
- – FA péri opératoire = Apparition FA en per opératoireo Surtout en chirurgie cardiaque
o ∅ essais larges pour guider la PEC
o Amiodarone → Médoc de prédilection - – FA post opératoire = Apparition FA en post-op immédiat
o Prévalence ⇒ Pic entre J2 et J4 post op
▪ Chez 20-50% en post op de chir cardiaque
▪ Chez 10-30% en post op de chir non cardiaque
▪ Chez 5-10% en post op vasculaire
o Bcp d’épisodes asymptomatiques (± résolution spontanée) o Cependant, FA post opératoire ⇒ Risque de
▪ Récurrences de FA +++
▪ AVC / Infarctus du myocarde
▪ Saignements
▪ Mortalité / Durée hospitalisation ▪ Infections
▪ Complications rénales
Prévention de la FA post opératoire
– β bloquants en péri opératoire
o ↘ risque de FA post opératoire (mais ↗ risque mortalité possible dans les essais)
o Equivalent à l’amiodarone selon des méta analyses
(mais association βBQ + Amiodarone est plus efficace)
- – Amiodarone faible dose (< 3 000 mg)o Effets indésirables faibles
- – Autres méthodes non prouvées (statines/magnésium/sotalol/colchicine/pericardiotomie postérieure/pacemaker atrial/corticoïdes) o ∅ effet des corticoïdes
o Colchicine ⇒ Essais en cours COP-AF
⇒ Recommandations
– R59 : Prévention FA post op de chirurgie cardiaque⇒ Donner en péri opératoire o Amiodarone
o β bloquants– R60 : Eviter βBQ pour prévention FA si pas de chirurgie cardiaque
– R61 : Patients avec FA post op sont à anticoaguler au long cours selon leur risque d’AVC
o Doivent être considérés chez chirurgie non cardiaque
o A considérer si chirurgie cardiaque
Diverses choses sur la FA
Prévention primaire de la FA
- – Identification et correction des FdR de FA +++
- – Traitement HTA / Insuff cardiaque
- – Essais en cours sur les ttt non AAR
⇒ Modifie substrat atrial pour éviter la FA (ou récurrence FA)Différences inter sexe dans la FA
- – Femmes sous représentées dans les essais
o Possible biais dans épidémio/physiopath/pronostic … o Recommandé de prendre des femmes dans les essais - – Caractéristiques des femmes ayant une FA
o Age plus élevé o ↗ fréquence de
▪ Patho valvulaire
▪ Insuffisance cardiaque à FEVG normale o ↘ fréquence des patho coronaires
o ↗ symptômes de la FA (et plus graves)
– Sexe féminin ↗ risque d’AVC sur FA
(mais que si présence ≥ 1 FdR)
o ↗ gravité et séquelles de l’AVC
o Anticoagulation moins contrôlable (sous AVK)
▪ ↗ risque d’AVC sous AVK ▪ Mais effet des AOD
– ↗ complication des AAR chez les femmes
o QTc allongé dans AAR classe Ia / III
o Dysfonction sinusale avec nécessité de pacemaker
– Fréquence d’utilisation des méthodes de contrôle FA o Moins de CEE
o Utilisation plus tard d’ablation de FA au cathéter
o Plus d’échecs de l’isolation des veines pulmonaires
(↗ complications)
o Plus d’ablation de NAV que les hommes
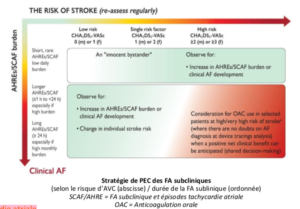
Episodes de FA sous clinique / tachycardie atriale (AHRE)
- – Incidence de FA sub clinique/AHRE = 30 – 70%
- – Durée de la FA sous clinique/AHRE
o Faibles durées (≤ 20 sec/jour) ⇒ ∅ effet clinique ▪ ∅ association à plus long épisodes
▪ ∅ association à risque embolique
o Durée plus élevée (≥ 5 min/j au total)
▪ ↗ risque de FA clinique
▪ ↗ risque embolique (et mortalité cardio vasc)
- – Si FA subclinique/AHRE ⇒ Apparition FA clinique
chez 20% des patients (dans ≤ 2,5 ans après début FA) - – Mais risque d’AVC bien inférieur si FA sub clinique/AHRE par rapport à FA clinique
o Présence FA subclinique/AHRE ≈ marqueur de risque o Cependant, il faut toujours traiter les facteurs
de risque d’AVC même si pas de FA
o Voire anticoaguler si durée FA subclinique/AHRE > 24h
avec risque élevé d’AVC
⇒ Recommandations
– R62 : Chez patients avec FA subclinique/Episode de tachycardie atrialedétectés par pacemaker/holter implantable ⇒ Faire
o Evaluation cardiaque : ECG + FdR CV + CHA2DS2VASc o Suivi du patient rapproché pour détecter▪ Progression vers FA clinique
▪ Durée des épisodes de tachycardie atriale/FA sub clinique(surtout si ≥ 24h)
Autres tachy-arythmies atriales (Flutter …) Flutter atrial
– Flutter peut être isolé
o Mais les patients développent souvent une FA après o Peut survenir chez ceux qui prennent
▪ Amiodarone
▪ AAR classe Ic
– Prise en charge thérapeutique identique aux patients FA +++
o Contrôle fréquence = 1ère étape
o Possible cardioversion en 1er (plus efficace ?)
▪ CEE ou stimulation haute fréquence
▪ AAR classe III (dofétilite / ibutilide)
- – Eviter les AAR classe Ic (flécaine/propafénone) sansbloqueurs du NAVo Risque de conduction flutter en 1:1 ⇒ Tachycardie
- – Ablation isthme cavo tricuspide au cathéter ⇒ Indicationso Flutter sur isthme cavo tricuspide identifié
o Flutter apparu sous amiodarone/AAR classe IcIndicateurs de bonne PEC d’une FA
- – Evaluation initiale du patient
o CHA2DS2VASc
o %tage de patient dont HAS-BLED est évalué régulièrement - – Anticoagulation
o %tage de patients anticoagulés sans raison parmi ceux
sans indication d’anticoagulation
(CHA2DS2VASc ≤ 0 (♂) / ≤ 1 (♀)
o %tage de patients anticoagulés parmi ceux ayant une
indication à anticoagulation (et sans refus)
- – Ralentissement FAo %tage de prescription d’AAR inappropriés parmi les patients en FA permanente (sans volonté de réduire la FA)
- – Réduction de la FA
o %tage de prescription d’AAR classe Ic parmi patients
avec anomalie structurelle cardiaque
o %tage d’ablation de FA par cathéter parmi les patients
avec échec/intolérance des AAR et symptomatiques
- – Contrôle des facteurs de risqueso %tage de patients dont FdR de FA modifiables sont identifiés (HTA / Obésité / SAOS / Abus d’alcool / Sédentarité Tabagisme / Mauvais contrôle glycémique)
- – Evolution / complications
o Nombre d’AVC/AIR
o %tage d’hémorragie graves parmi les patients anticoagulés
Autres tachy arythmies
– Flutter atypique = Tachycardie atriale par macro réentrée o Survenue sur cœur malade ++
o Traitement identique aux flutter MAIS
▪ Utilisation AAR plus difficile (cœur non sain)
▪ Ablation plus complexe
– Flutter atrial (± atypique) en post ablation de FA par cathéter
o Préférer contrôle fréquence / AAR
⇒ Résolution souvent spontanée de ces épisodes
o Traitement de cette récurrence à faire plus tard si ∅ résolution





 21 janvier 2021
21 janvier 2021